正文
目的:
为我国制药企业药品研发质量管理体系的建立和完善提供建议与思考。
方法:通过分析我国和美国FDA药品监管机构的检查报告、访谈我国制药企业研发质量管理负责人,了解我国制药企业研发质量管理的现状,为药物研发质量管理体系的建立和完善提供建议。
结果与结论:完善的药品研发质量管理体系应包括以下几点:①设立独立的研发质量管理部门并充分赋权;②分类建立文件体系,使质量管理有章可循;③加强培训,确保培训效果;④建立有效的质量考核管理制度,确保质量体系有效运行。
正文:
药品质量体系(Pharmaceutical Quality System,PQS)是为在药品质量方面指导和制药公司为控制药品质量而建立的管理体系[1],质量管理体系通过对产品的整个生命周期(包括药品研发、技术转移、商业化生产和产品退出市场)中影响产品质量的所有因素进行管理[2],从而对产品的质量提供全面有效的保证,实施全生命周期的质量管理,对于药品质量至关重要。
人用药品注册技术要求国际协调会(International Conference on Harmonization,ICH)发布的ICH Q8、ICH Q9、ICH Q10和ICH Q11[3-5],是药品从研发到生产的质量管理体系的基本纲要和管理的基础,为药品研发和监管决策提供了基于科学和风险的方法[6],对于指导整个制药行业全面理解药品全生命周期质量管理具有重要意义。随着中国加入ICH以及ICH相关指导原则在中国相继执行,中国药品监管机构也相继出台了一系列药品研发质量相关的文件;
2015年7月22日,原国家食品药品监督管理总局(China Food and Drug Administration, CFDA)印发《关于开展药物临床试验数据自查核查工作的公告(2015年第117号)》 [7];2016年5月4日,CFDA发布《化学药品新注册分类申报资料要求(试行)2016年第80号》 [8],该文件加强了对临床数据真实性的监管及加强了申报者对资料的负责度要求,数据真实性要求更严格;2017年8月2日,CFDA发布了新版《药物非临床研究质量管理规范》(国家食品药品监督管理总局令第34号)[9],其中,再次强调了数据管理和计算机化系统的规范管理;
2018年1月15日,国家药品监督管理局(National Medical Products Administration, NMPA)发布了《药品数据管理规范(征求意见稿)》 [10],该文件是对新版《药品生产质量管理规范》的一次多向的延伸,对药品全生命周期的数据管理做出了全面的规定,是一个针对药品全生命周期管理的数据管理规范。中国的制药行业必须将监管法规及指导原则应用到实际工作中,建立完善药品研发质量管理体系,保证药品研发质量。
目前,我国制药企业药品研发阶段的质量管理一直处于探索阶段,研发质量管理体系亟待完善。因此,制药企业建立一套科学、合规的药品研发质量管理体系非常有必要。本文针对我国目前药品研发质量管理的现状,分析研发阶段质量管理存在的具体问题,为完善研发质量管理体系、提升药品研发质量提出建议。
1 我国药品研发质量管理存在的问题
通过对监管机构官方检查报告进行分析,梳理出药品研发过程中由于质量管理缺陷引起的药品研发质量相关问题。然后又进一步调研了多家大、中、小型制药企业质量管理负责人,对企业内部药品研发过程中出现的质量管理问题进行汇总。通过对以上问题进行深入分析,发现药品研发过程中的质量管理主要存在以下问题。
1.1 监管机构检查发现的药品研发质量管理存在的问题
笔者梳理了2015-2017年CFDA的食品药品审核查验中心发布的《药品检查报告》 [11-13]和2013- 2018年美国FDA给中国企业发布的警告信[14]中关于研发阶段的药品质量相关问题,发现数据真实性问题较为突出,主要体现在实验记录、工艺研究、物料管理、偏差处理和计算机化系统验证等方面。
1)实验记录:原始记录不完整,缺少仪器使用记录,图谱信息不完整,无电子图谱,缺少对照药品来源证明,有誊抄记录现象,隐瞒合作研究单位等。实验室的研究记录与申报资料的内容、格式完全一致,没有失败的实验记录,无法体现研究探索过程。
2)工艺研究:工艺验证出现偏差时,未能及时进行记录和分析,没有找到根本原因,未能制定预防和纠正措施。关键性临床研究的样品与注册申报的商业化生产工艺存在显著性差异,药学变更的影响评估不充分。
3)物料和样品管理:原辅料来源和使用记录不完整,未能提供原辅料来源的凭证,未对原辅料供应商进行质量稽查,未进行检验;试制样品管理混乱;未能按规定留样并进行稳定性考察。
4)偏差处理:在出现偏差、超标结果时没有及时调查,或者调查不深入、不全面,没有对产生偏差的根本原因进行充分的调查。
5)计算机化系统验证:部分企业没有建立研发体系的计算机化系统管理规程,没有对计算机化系统验证、电子数据的采集、备份和还原、系统安全等制定相关的管理规范,计算机化系统人员的权限设置不合理。
1.2 企业调研发现的药品研发质量管理问题
笔者访谈了10家不同规模的制药企业研发质量负责人,并根据从业人员、营业收入和资产总额分为大、中、小型,其中大型企业3家,中型企业4家,小型企业3家,对药品研发过程中出现的质量管理问题汇总如下。
1)未建立研发质量管理部门:其中部分小型企业未建立独立的研发质量管理部门,没有开展研发质量管理工作或由研发人员或项目管理人员兼任该项工作,当出现研发质量有关问题时,可能会出现以牺牲质量来换取研发项目进度的情况。
2)虽已建立质量管理部门,但是制度不完善;有些中型企业成立了研发质量管理部门,但缺少足够的授权,导致在实际工作中研发质量管理部门形同虚设,在实际工作中,项目负责人和部门负责人的权力大于研发质量负责人;有的企业虽然成立了研发质量管理部,但照搬《药品生产质量管理规范》(GMP),未根据研发不同阶段的实际情况和特点针对性地建立研发质量管理体系,导致研发效率低下。还有一些企业建立了研发质量管理体系,但是,相关制度不完善,比如缺少技术转移过程中相关流程和规范,导致技术转移不畅、研发和生产体系相互推诿责任等。
3)研发质量管理执行不到位:研发人员对质量管理的理解不深刻,在药品研发过程中质量管理规范执行不足、原始记录不规范、偏差及超标调查不充分等问题突出。研发人员质量管理意识淡薄,缺少相应的管理和制度来从根本上提升研发人员的质量意识和行为。
4)未能厘清技术问题和质量管理问题:部分企业在前期研究不足,产品工艺开发过程不充分,药品工艺验证方案设计不科学,这些问题实质是技术问题,而非质量管理的问题。
2 如何建立完善的药品研发质量管理体系
虽然目前没有明确的法规要求研发阶段必须建立质量管理体系,研发机构可以根据自身规模和组织架构,结合所开发项目的特点,构建相应的研发质量管理体系,制定相关管理制度,保证体系的建立和执行到位。
2.1 设立独立的研发质量管理部门,明确相关职责并充分赋权是履行研发质量职责的保障
制药企业应当设立独立于研发和生产体系的质量管理部门,从公司管理制度上确保质量管理部及其部门负责人的权力,以便充分发挥质量管理部门的监督和管理作用,促进质量管理体系相关制度的执行。制药企业组织架构见图 1。
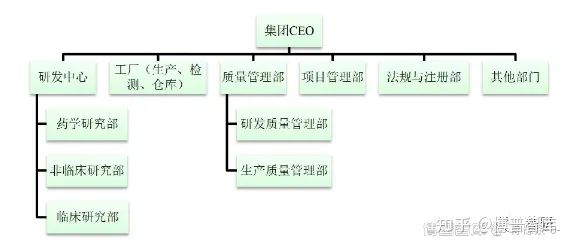
图 1 制药企业组织架构示意图
药品研发质量管理部门的具体工作职责主要有以下内容:
1)建立并不断完善药品研发质量管理的文件体系。例如制定研发质量管理的方针、政策和质量手册、程序管理类(Standard Management Procedure,SMP)及标准操作规程(Standard Operation Procedure,SOP)等文件;负责建立档案管理工作。
2)实施和持续改进研发质量体系并保证其在不同研发阶段的质量符合性。监督和检查所负责项目研究节点的进度及该节点研究文档的合规性(符合性/数据真实性);审核所负责项目的实验方案和质量标准、检验规程;对所负责项目在药品注册研制现场核查前模拟药品研制现场核查;组织内部稽查等质量管理活动,批准稽查方案、报告,并确保适当的纠正和预防措施得到执行;管理实验室与所负责项目的相关偏差、变更;定期检查所负责实验室的基础质量管理,例如研发计量器具检定、外部校准工作等。
3)临床研究用样品的管理。确保临床研究用药品符合质量标准,经过检验放行后方可使用;负责临床研究用样品生产、包装过程的质量监管和最终样品的批放行,以保证临床试验受试者的安全。
4)确保验证工作的完成。临床样品和申报批的生产及检验、分析方法验证等过程所涉及的验证工作应按照GMP要求开展,对验证方案和报告进行审核和批准,保证验证方案的合理性,并对验证文件进行归档管理;对完成的验证报告进行审核,保证各阶段验证报告数据的真实性,能够对验证过程中发生的偏差,按照偏差处理报告的方式进行跟踪处理;下达年度验证计划,对上年度验证情况进行总结,能够按照每年的验证计划对每个验证的进度进行跟踪和管理。














