正文
至于资金方面,如果在申请中包括中国法规,可以大大提高吸引风险投资的可能,如果有本地合作伙伴,甚至可以吸引公共政府引导基金。无论你听到的中国经济怎样,中国基金中还是有丰厚的来自私人和政府的资金。在有的省份,生物技术初创企业能够获得超过1000万人民币(140万美元)政府/公共资金。
中国风险投资企业也在美国和欧洲成立了公司,在世界范围内,增加对早期生物技术企业的投资,尤其是对可以符合中国法规的项目。
从研发企业数量上看,中国已经取代日本,成为亚洲最大的新药研发国。国内新药研发企业已在质变前夜。随着CFDA和CDE不断的政策支持和持续的理念更新;随着海外人才的陆续回归与新药研发配套产业的完善;随着整体工业水平的提升与部分新药研发相关领域技术(如基因测序、分子诊断和精准医疗)的迅猛发展,随着风险投资机构的前瞻性及专业化程度大幅提升等因素,新药研发(开发)行业即将进入质变的快速生长期。面向中国甚至全球市场,掌握重磅产品和关键技术的平台型新药研发企业及临床优势明显的重磅品种将受到资本的青睐。
全新靶点及化合物的原创新药研发具有很高资金成本和研发风险,而引进重磅品种并进行差异化和针对性地开发或具有更为可控的资金成本和研发风险。
这样的思路催生了两方面的趋势:一方面,外资药企出于合规风险及药物推广成本的考虑倾向出售药物的中国区授权。而国内药企在合规和低成本营销方面具有独特优势,获得外企的独家授权可以迅速增强竞争力。新药研发未来趋向于精细和精准。化学创新药通常有效性高,广谱性高又易于口服,但随之而来的副作用也会较大;生物药靶向性更好,安全性高,但有效性不足,且通常不能口服。发展兼顾两者优势的新药会成为趋势,如小分子药物的新剂型(缓释、靶向)或生物药的新品种(长效、口服)等。
近年来在发达国家生物药研发领域的异军突起是多种原因决定的:
(1)化学药研发成功率降低,均摊成本显著提高。
(2)生物药的高安全性导致高研发成功率。
(3)发达国家社会支付体系完善。
而对于国内新药研发企业而言,化药总体研发成本(尤其是临床实验成本)较低, Me too Me better类新药可借鉴大量国外经验,显著提高成功率,药价可被国内大部分人群接受,所以国内化学新药的研发仍存在很多机会。而对于国内生物创新药来说,成本及价格过高,在支付端受限或成为制约其发展的关键因素。当前在较高行业预期的情况下生物创新药的市场仍将持续火热,但未来必将经受市场考验。
1990年人类基因组计划正式启动,1999年7月7日,中国申请加入该计划,并作为最后一个贡献者,承担3号染色体短臂一侧约30cM区域的测序和分析任务。
2000年6月,“北京区域”的草图与人类全基因组序列草图同步完成,该区域至今仍是人类基因组参考序列中最为准确的区域之一。中国和中国企业的参与,从此改变了生命科学的国际合作格局。参与人类基因组计划是我国生命科学发展中的一个里程碑和新的起点,以该计划为起点,我国在这一新兴的重要科技领域,几乎与世界同步发展。
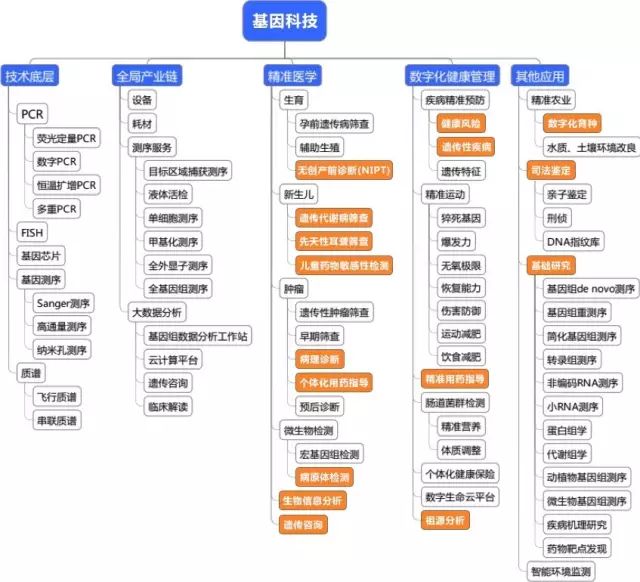
此后中国还做为主要发起国和参与国,开展了10%国际单倍体型计划、国际千人基因组计划、国际癌症基因组计划、水稻和家蚕基因组计划、META基因组、“生命之树”与动植物基因组、第二代酵母全基因组设计和合成等项目。
人类基因组计划的成果极大的促进了医学与基因组学的交叉融合,近两年发展迅速的精准医学就是建立在当时成果基础之上的。随着新一代测序技术的不断迭代,基因捕获技术、生物信息学、基因编辑技术的不断成熟,精准医学也逐渐从概念走向成熟。
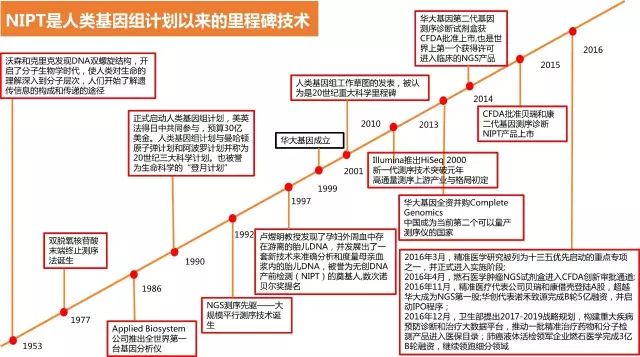
素材来源 华大基因 测序技术简史 修改
无创产前筛查(NIPT)是人类基因组计划以来的里程碑技术,是从科学发现、技术发明到产业发展的经典案例,从无到有创造了一个千亿规模的市场,中国基因测序的行业引领者华大基因、贝瑞和康已经成为NIPT领域的全球龙头企业。
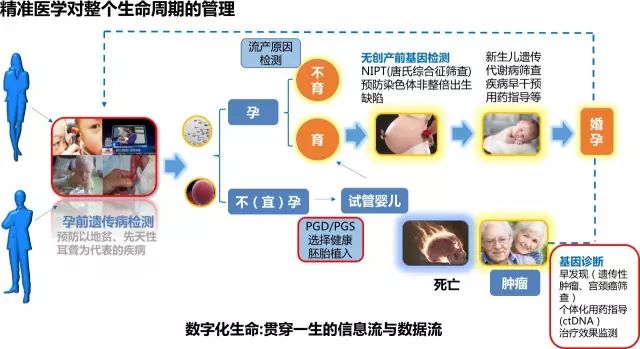
目前精准医学临床应用最多的是肿瘤的精准用药及复发监测。通过肿瘤的分子病理学检验加上高通量测序、单细胞测序等技术,从分子的层面解释患者的个性化情况,从而在临床上制定精准的治疗方案与了解预后情况,结合靶向药物、细胞治疗等手段,实现精准与个性化的治疗。
目前,国内的NGS与ctDNA领域竞争局面经过最近两年的跑马圈地,2017年行业或将迎来洗牌期和更残酷的竞争。企业方面,处于领先地位的燃石医学、世和基因、泛生子等企业持续得到资本关注。短期内关注各家的商务拓展及商业化落地能力,中期看服务质量和产品研发与报证能力及客户粘性,长期将看大数据的积累应用、商业生态的打造及新技术的开发与商业化。
美国作为基因测序技术的发源地,Illumina公司旗下癌症早筛公司Grail获得9亿美元的B轮融资之后不久宣布与无创DNA产前检测奠基人卢煜明教授创办的Cirina公司合并。癌症早筛的重要性不言而喻,未来结合人工智能诊断等技术,一个万亿级的蓝海市场正在喷薄而出。
癌症早筛的发展主要依赖于液体活检,DNA捕获与扩增等技术,甲基化及其他靶点的发现等技术的发展,同时也需要积累足够的临床数据,具备明确的临床指证,才能逐渐成为早期筛查的金标准。预计国内该领域也将诞生一批创业公司。
2017年5月24日,美国FDA批准默沙东(MSD)的KEYTRUDA(pembrolizumab)治疗带有微卫星不稳定性高(microsatellite instability-high,MSI-H)或错配修复缺陷(mismatch repair deficient,dMMR)的实体瘤患者。值得一提的是,这是美国FDA批准的首款不依照肿瘤来源,而是依照生物标志物进行区分的抗肿瘤疗法,具有里程碑式的意义。
MSI-H与dMMR是两种常见的遗传异常,含有这两种变异的肿瘤,细胞内的DNA修复机制往往会受到影响,不能正常发挥作用。带有这些异常的肿瘤分布非常广泛,可出现在结直肠、子宫内膜、胃肠道、乳腺、前列腺、膀胱、甲状腺等多个部位。因此,通过遗传变异特征而非病发部位来区分这些癌症,对于治疗有着更好的指导意义。
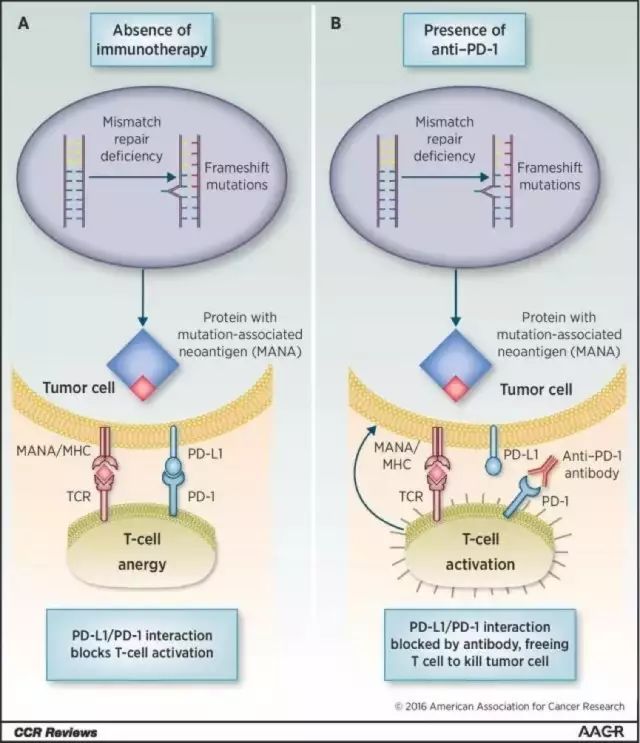
肿瘤免疫疗法对带有特定遗传变异的肿瘤有着很好的疗效
图片来源:《Clinical Cancer Research》
精准医学指导下的药物开发是以个体化医疗为基础,交叉运用基因组测序技术以及生物信息大数据技术从而开发特定患者的特定的基因突变的靶向药物市场。精准医疗的出现导致疾病的分型更加的细化,疾病亚群数量大量增加,大型制药公司很难再完全垄断创新药研发的市场,同时与传统药物研发模式相比以精准医疗为指导的新药研发可以显著降低研发成本和周期,提高临床成功率。掌握核心技术的中小企业和初创公司面临更多机会,也能对新趋势实现快速反应,更具投资价值。
参考文献:
基因泰克:生物技术王国的匠心传奇 作者:【美】萨莉·史密斯·休斯. 中国人民大学出版社出版.2017年03月
2017中国医疗健康产业投资白皮书 |【易凯行研报告】
硅谷银行医疗健康行业投资与退出趋势报告(2016年回顾与2017年预测)
《Chinese CROs for accelerated and cost-effective early-phase drugdevelopment programs: considerations for emerging biotech》Harri Jarvelainen PHD

本文为“星河融快(公号ID:rongkuai888)”在Xtecher官网平台(www.xtecher.com)的投稿。
星河融快(ID:rongkuai888)将通过专业的分析,持续与你分享“有趣的”产业互联网干货。欢迎你在下方留言和我们分享有趣的观点,自荐或推荐优质产业互联网项目,同时也欢迎你来上地18号和我们聊聊。
━━━━━
封面来源:网络 排版:陈光 校对:陈光
━━━━━
Xtecher官网平台现开通认证作者,
有发稿意向的个人或媒体,可联系微信:
jueshao121
(添加好友请注明公司、职位、事由)
点击
|
关键词
|
查看对应内容