正文
现在研究较多的假说为病毒学说,病例报告中报道过单纯疱状病毒感染和EB病毒感染,抗体形成, 多单侧发病,病毒基因整合到人类基因进行表达。
病理生理
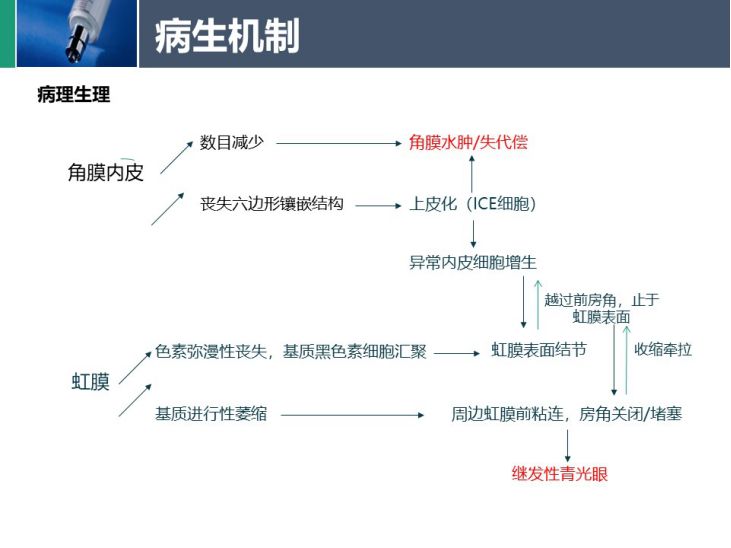
三种不同类型ICE综合征共同的潜在机制是角膜内皮的异常,即上皮化,形成ICE细胞。显微镜检查发现,角膜内皮细胞的数量减少、呈现出多形性,并伴有明暗反转(细胞边界较亮、细胞表面较暗)。这些异常的内皮细胞还获得上皮细胞的特征,例如桥粒、胞质内细丝和微绒毛的存在。异常的内皮细胞可以作为膜在相邻结构上迁移,包括虹膜和小梁网,越过前房角,止于虹膜表面,还可形成虹膜表面结节。而且,异常的内皮细胞还被证明可以分泌异常的基底膜、类似于Descemet膜。这种膜的收缩导致相关的虹膜变化、虹膜粘连和房角关闭等,导致继发性青光眼。
流行病学
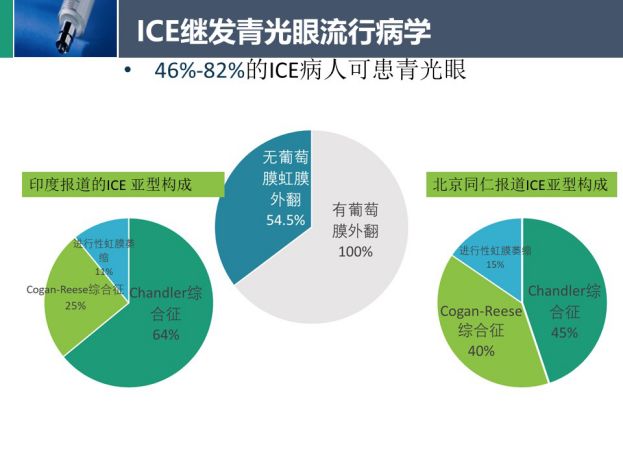
ICE导致房角关闭和眼压升高,约46%~82%的ICE患者可患青光眼,以闭角性青光眼多见
6
。塞尔维亚的一项研究
7
,报道了有葡萄膜外翻和没有葡萄膜外翻的ICE患者的继发青光眼患病率,分别为100%和54.5%。Chandran等人对203名印度ICE患者进行回顾性研究
8
发现继发青光眼患病率为73%,其中54%的虹膜进行性萎缩(PIA)、47%的Cogan Reese综合征和45%的Chandler综合征患者需要进一步手术治疗。Bo Feng等人在中国北京的研究
9
中,调查了58个ICE患者,发现继发性青光眼患病率达到98%,其中包括Chandler综合征(44.9%),Cogan-Reese综合征(39.7%)和PIA(15.5%)。
印度的研究表明PIA导致的难治性青光眼比CS和CRS更多,治疗也更困难。而在中国发病率更高的为Chandler综合征。
治疗方法
目前ICE的治疗方法主要包括药物治疗、手术控制眼压和角膜移植三个方面。药物治疗包括控制眼压(偏向应用抑制房水生成的药物,包括α受体激动剂、β受体抑制剂、碳酸酐酶抑制剂等,通常与缩瞳剂联用);缓解角膜水肿和维持角膜透明度(如高渗剂:高渗盐水、甘油、甘露醇等,配戴角膜软镜并配合抗炎治疗);抗病毒治疗。手术控制眼压的方法包括小梁切除术、引流阀植入术、睫状体光凝术。角膜移植包括全角膜移植、内皮角膜移植等。
小梁切除术联合抗代谢物对于Chandler综合征治疗效果最好,对Cogan-Reese综合征手术效果尚可,进行性虹膜萎缩最差。引流植入术相对于小梁切除联合抗代谢治疗在近期的成功率较低,在长期的成功率较高。
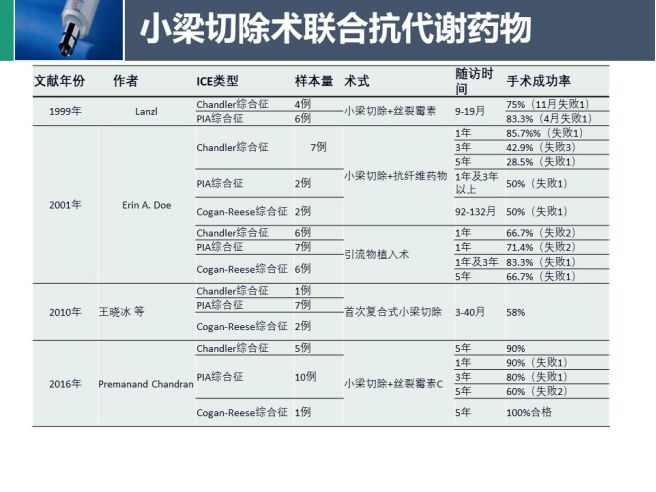
如同其他继发性青光眼手术一样,ICE综合征患者手术控制眼压也会存在手术失败的情况。对于滤过手术,其失败有关的因素有:内皮细胞持续增长阻塞滤过部位、结膜下和巩膜滤过通道纤维瘢痕化情况、ICE患者年龄(相对年轻)。与引流装置植入术失败有关的因素包括ICE膜情况和角膜失代偿情况;手术失败后如需要重新置管,建议:①延长管道,使管道固定在巩膜上 ②植入更深眼内,远离角膜内皮和虹膜。
那么,是否存在一种较好的治疗办法呢?穿透性粘小管成形术是一种可以在保留虹膜角膜粘连的情况下非滤过泡依赖的手术方式,术后Schlemm管引流不发生瘢痕问题。但该方法是否提高了手术的成功率尚需要进一步研究。
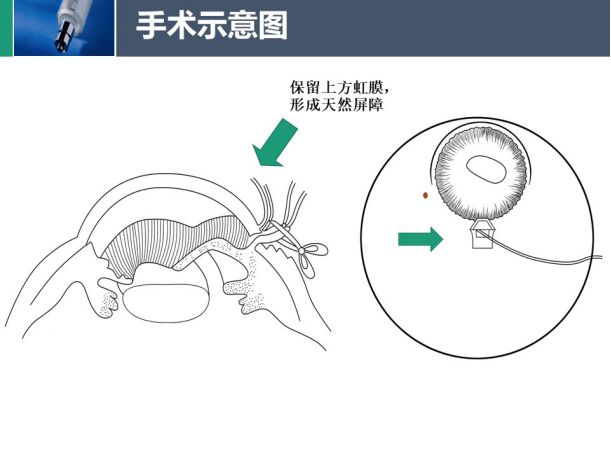
男性,43岁,因“左眼虹视5年,视物不清4月”就诊。















