正文
100 mL
梨形瓶中,加入
10 mL
二氯甲烷溶解,再称取处方量的蝙蝠葛碱加入到上述溶液中溶解,将梨形瓶固定到旋转蒸发仪上,在一定水浴温度下旋蒸挥干二氯甲烷,在瓶壁内侧形成一层透明薄膜,减压干燥
1 h
,放入到真空烘箱中过夜;加入去离子水
50 mL
水化薄膜,并保持外界水浴温度与内水相温度一致,同时进行磁力搅拌,速率为
500 r/min
,持续水化搅拌
30 min
,即形成淡蓝色溶液,样品溶液经
0.45 μm
微孔滤膜滤过,并加入去离子水至体积为
50 mL
,即得到
Dau-CNMs
(加
TPGS
)或
Dau-SNMs
(不加
TPGS
)。
2.2
包封率测定
取
Dau-CNMs
或
Dau-SNMs 2.0 mL
加入到截留相对分子质量为
10 000
的超滤离心管上端,密封,放入到离心机中,在
5000 r/min
下离心
20 min
,收集离心管底端中超滤液置
10 mL
量瓶中,加入流动相定容(
W
游离
);另取
Dau-CNMs
或
Dau-SNMs 1.0 mL
置
50 mL
量瓶中,加入乙腈
5 mL
,水浴超声
5 min
,加入流动相定容(
W
总
)。检测上述
2
种溶液中的药物含量,并计算药物包封率:
包封率=
1
-
W
游离
/
W
总
2.3 Dau-CNMs
处方筛选
2.3.1
临界胶束浓度(
critical micelleconcentration
,
CMC
)测定
聚合物在溶液中的浓度只有超过
CMC
值才能形成胶束,而具有较低
CMC
值的聚合物其形成的胶束在进入体内后可避免由于体液稀释而破坏其完整性
[17]
,因此,
CMC
成为评估胶束稳定性的重要参数。
本研究采用芘荧光光谱法测定单一或复合聚合物的
CMC
值
[18]
。具体操作如下:配制浓度为
6 μmol/L
芘的丙酮溶液,精密移取
0.1
~
10 mL
棕色量瓶中,氮气吹干丙酮,平行制备
7
份样品;另按照表
1
的处方配比配制一系列质量浓度的单一或复合聚合物溶液,加入到上述含芘的量瓶中,定容,使芘在各聚合物样品中的浓度为
0.06 μmol/L
,每个量瓶中放入一个磁力搅拌子,持续搅拌
48 h
确保平衡,分别取样测定各样品溶液进行荧光光谱法扫描,记录第
1
特征峰
373 nm
与第
3
特征峰
384 nm
的荧光强度(
I
)之比(
I
373
/
I
384
),聚合物的
CMC
值由荧光强度比(
I
373
/
I
384
)与聚合物质量浓度对数值(
lg
C
)的关系图中的交叉点确定,不同配比
Soluplus
®
与
TPGS
形成的
CMC
值见表
1
。
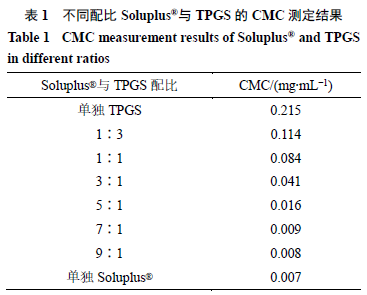
从实验结果可知,
TPGS
具有较高的
CMC
值,为
0.215 mg/mL
,形成胶束需要
TPGS
质量浓度较大;而
Soluplus
®
具有极低的
CMC
值,为
0.007 mg/mL
;另外,随着
Soluplus
®
与
TPGS
的配比由
1
∶
3
增加到
9
∶
1
,形成的复合纳米胶束的
CMC
值逐渐降低,说明其形成胶束逐渐具有了较强的抗稀释能力和稳定性。
2.3.2
纳米胶束制剂性质研究
胶束具有极小的粒径分布,可显著提高难溶性药物溶解度,并容易透过细胞膜,是提高生物利用度极具有前途的口服给药系统
[19]
。按照“
2.1
”项下方法制备
Soluplus
®
与
TPGS
不同配比的蝙蝠葛碱纳米胶束,并评价制剂学性质,结果见表
2
。

由实验结果可知,单独以
TPGS
制备的胶束(
Dau-SNMs
)粒径较大,这是由于
TPGS
的
CMC
值较高,溶液中需要较高质量浓度的
TPGS
才能形成胶束,因此,
TPGS
形成的纳米胶束粒径较大
[20]
;而相反,
Soluplus
®
具有极低的
CMC
值,在较低的质量浓度下即可形成纳米胶束(
Dau-SNMs
),因此
Soluplus
®
形成的纳米胶束粒径较小
[21]
;
Soluplus
®
与
TPGS
的配比由
1
∶
3
增加到
9
∶
1
,形成的
Dau- CNMs
的粒径和
PDI
均呈减小趋势,在
Soluplus
®
与
TPGS
配比为
7
∶
1
时制备的复合纳米胶束粒径较小,而包封率随着
Soluplus
®
与
TPGS
的配比的增加而增大;
Soluplus®
与
TPGS
的配比对复合纳米胶束的
Zeta
电位影响较小。
2.3.3
药物泄漏率测定
胶束在进入体内被体液稀释后药物可能会发生泄漏,尤其是对于弱碱性药物,泄漏的药物在进入肠道中有可能析出药物沉淀,不利于药物吸收,影响药物生物利用度
[8]
。为了考察
Dau-CNMs
和
Dau-SNMs
在胃肠道环境中的药物泄漏率,分别选择
pH 1.2
盐酸溶液和
pH 6.8
磷酸盐缓冲液作为模拟介质进行药物泄漏率考察,具体操作如下:取不同配比
Soluplus
®
与
TPGS
形成的
Dau- CNMs
以及
Dau-SNMs
各
5 mL
,分别加入到
pH 1.2
盐酸溶液和
pH 6.8
磷酸盐缓冲液介质中,体积均为
50 mL
,放置在
37
℃水浴中持续振荡。在
pH 1.2
盐酸溶液介质中的样品振荡
2 h
后取样,经超滤离心,取超滤液测定游离药物含量
[22]
;而在
pH 6.8
磷酸盐缓冲液介质中的样品振荡
24h
后取样,在转速为
5000r/min
下离心
20 min
,取上清液
1 mL
加入到
10 mL
量瓶中,乙腈破乳并定容,检测药物含量,计算药物泄漏率
[22]
,结果见表
3
。

通过实验结果可知,在
pH6.8
磷酸盐缓冲液中不同配比的
Dau-CNMs
的药物泄漏率随着
Soluplus
®
与
TPGS
配比的增加而降低,即
Soluplus
®















