2017年7月31日,化合物KPM-2有望用于肿瘤和神经退行性疾病的治疗
NAD依赖的蛋白去乙酰化酶SIRT2属于组蛋白去乙酰化酶家族,尽管其在神经细胞和肿瘤细胞中的功能还没有被完全揭示,但由于它被认为与肿瘤和神经退行性疾病相关联,故针对SIRT2抑制剂的研究具有重要意义。来自Ono Pharmaceutical公司的研究人员和合作者们基于对化合物与SIRT2蛋白的复合物X-ray晶体结构研究发现了一个全新的抑制剂KPM-2。该化合物能够结合在SIRT2的活性位点而发挥活性,形成稳定的KPM-2-ADP-ribose复合物,竞争性的夺取NAD+与蛋白的结合。KPM-2可以抑制癌细胞的增殖和促进神经突起生长。研究结论显示,KPM-2有望用于肿瘤和神经退行性疾病的治疗。(Itoh, Y. et al. 11th AFMC Int Med ChemSymp (AIMECS) (July 23-26, Melbourne) 2017, Abst).
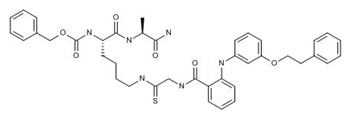
图为KPM-2结构
2017年7月18日,FDA批准Nerlynx用于早期 HER2 阳性乳腺癌的延长辅助治疗
FDA批准了Puma Biotechnology 公司的Nerlynx(来那替尼,Neratinib,曾用代号PB-272),一个日服一次的口服酪氨酸激酶抑制剂,用于成人早期受体酪氨酸激酶ErbB-2阴性/HER2 阳性的乳腺癌在服用曲妥珠单抗(Trastuzumab)后的延长辅助治疗,并将于今年九月份上市。该药的获批基于一项名为ExteNET的有安慰剂对照的多中心随机双盲III期临床试验结果(ClinicalTrials.gov编号NCT00878709)。该研究针对2840 名在2年内使用过Trastuzumab 治疗的HER2 阳性的早期患者进行了为期1年的随机分组治疗:Neratinib组1420人和安慰剂组1420人。两年后的随访表明,94.2%的Nerlynx治疗患者未经历癌症复发或死亡,而安慰剂组的这一比例为91.9%。Neratinib的常见副作用(> 5%)包括腹泻、恶心、腹痛、疲劳、呕吐、皮疹、口腔炎、食欲减退、肌肉痉挛、消化不良、AST 或 ALT 酶升高、指甲疾病、皮肤干燥、腹胀、体重减轻和尿路感染。Neratinib用药组有16.8%由于严重腹泻造成治疗中止,这是导致治疗中止的最普遍副作用。患者在接受Nerlynx 治疗的前 56 天应使用洛派丁胺治疗腹泻,之后按需使用。另有1.7%的用药患者出现肝毒性或转氨酶水平上升。该药目前已提交欧盟并正在评审过程中。(Puma Biotechnology公司新闻稿;FDA新闻稿)。





