正文
2007年9月该药在欧洲获得治疗晚期软组织肉瘤的许可。Yondelis®是一种全新的、多模块合成的抗癌药,最初从海鞘身上提取制得。该药物通过不同的药物作用机制阻止肿瘤发展,包括捆绑DNA(脱氧核糖核酸)阻止细胞再生、抑制活化转移和蛋白质参与DNA修复、改变肿瘤微环境。
2009年9月Yondelis®获得了欧洲药品局医药产品委员会人类卵巢癌使用的积极推荐,该药当前与强生的聚乙二醇脂质体Doxil(阿霉素)组合用于治疗卵巢癌,2009年11月2日Yondelis®和Doxil以联合疗法治疗卵巢癌获欧洲监管机构批准上市,这一新的适应症的获批也是众望所归。
该组合药已被批准在包括挪威、冰岛以及列支敦士登在内的27个欧盟国家上市。但是其首批投放的国家有英国、澳大利亚、德国、丹麦、瑞士、芬兰以及挪威等。现在Yondelis®在全球77国家中均有销售,是一种用于治疗晚期软组织肉瘤的单一药物;在70个国家中它与Doxil一起治疗复发的铂敏感卵巢癌。
与欧洲大相径庭的是,2009年9月美国FDA因为安全问题过大和疗效并不显著等原因拒绝了Yondelis和Doxil联合疗法的上市申请,其中包括该公司正在进行的关键试验,以及进一步临床药理学研究的总体生存率数据。两年后因为同样原因,公司被迫暂停了这一项目并将其转向恶性肉瘤的研发。
2014年11月24日,PharmaMar在美国研发Yondelis®的战略合作伙伴Janssen Research & Development(杨森研发有限公司)提交了新药上市申请。2015年2月4日PharmaMar对外宣布美国FDA同意优先审核Yondelis®用于包括脂肪肉瘤和平滑肌肉瘤亚型在内的晚期软组织肉瘤(STS)患者的新药上市申请(NDA)。这些患者前期曾接受过
一种
含蒽环类药物的治疗。
2015年10月23日,美国食品药品监督管理局(FDA)批准化疗药Yondelis®用于治疗不可切除的或晚期(转移性)脂肪肉瘤和平滑肌肉瘤,获批的两项适应症是这种肿瘤中恶性程度较高的类型,其适应人群是既往接受过蒽环类化疗药物治疗的患者。
ET-743是一个分子中含有3个四氢异喹啉单元,8个环以及1个含半胱氨酸残基的10元内脂杂环,7个手性中心的复杂生物碱类化合物。Kerr等通过标记氨基酸证明其生物合成途径是来源于两分子络氨酸缩合成环二肽,后经过氧化为羟基二酮哌嗪类化合物,从而结合进入到ET-743分子中。
ET-743的各项研究开展后,就需要持续不断的生产,科学家们通过系统的研究,于1996年,Corey等首次报道了ET-743的全合成,但经过30多步反应得到目标产物,总收率仅为0.75%。2000年Corey对之前自己课题组报道的路线进行了优化,提高了收率,适用于工业化生产。实际上,Trabectedin(曲贝替定)的来源是通过其类似物Cyanosafracin B半合成而来,而Cyanosafracin B由生物发酵法获得公斤级的产物。
ET-743抗肿瘤的作用机制独特而复杂,参与了多种机制:可以使DNA双螺旋小沟处的鸟嘌呤的N-2烷基化,阻断DNA的复制与合成,抑制肿瘤细胞的分裂生长;抑制遗传修复途径;干扰细胞周期导致p53依赖性的程序性死亡,扰乱肿瘤细胞微观网络;在DNA和拓扑异构酶Ⅰ之间引起交联。如下图所示:
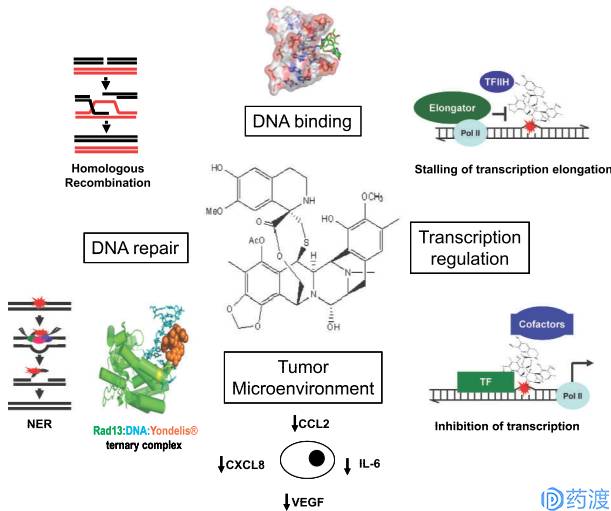
曲贝替定(Yondelis,trabectedin,ET-743)的抗癌作用机制





