正文
]
。
以上这些长效的病毒疫苗往往具有一个共同的特点,就是通过
诱导机体产生中和抗体
来抵御病毒的入侵。对于急性感染的传染病来说,这一点显得尤为重要。
具体来说,长效疫苗可以诱导人体的免疫系统产生出长效浆细胞和记忆B细胞。长效浆细胞可以长期产生抗体;记忆B细胞虽然不直接制造抗体,但可以长期保持对该病毒的“记忆”,一旦发生病毒入侵,记忆B细胞就会被激活产生浆细胞,从而分泌大量中和抗体来对抗病毒。中和抗体可以紧紧附着在病毒表面,阻止病毒与人体细胞结合
(图1)
;有的中和抗体即使在病毒与细胞发生接触以后,仍然可以阻断病毒释放遗传物质进入细胞,从而防止病毒感染。
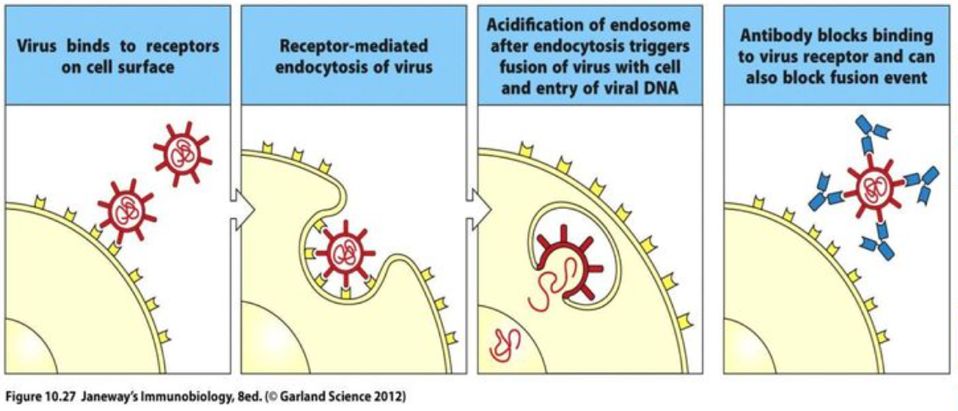
图1. 中和抗体阻断病毒感染示意图。图中红色表示病毒,黄色表示细胞,细胞表面黄色突出状表示细胞表面受体。病毒感染过程中首先通过膜蛋白与细胞表面受体结合(A),之后通过细胞内吞作用进入细胞(B) ,随后释放遗传物质进入细胞(C)。当体内存在中和抗体时,中和抗体可以紧密结合在病毒膜蛋白表面,从而阻止病毒与细胞受体结合(D)。图片来源自Janeway's Immunobiology, Ninth Edition.
一项研究表明,注射乙肝疫苗免疫30年后,再进行一针免疫,有88%的受试者可以产生高滴度的抗体,这证明乙肝疫苗诱导出的记忆B细胞可以提供长期保护
[5
]
。另一个经典的案例是黄热病疫苗,YFV-17D,一针免疫40年后,接种者体内仍然存在特异性抗体
[6
]
。目前,上市的绝大多数病毒疫苗都是通过诱导高滴度的中和抗体来保护人体免受病毒感染。
第一是技术上的原因。
与上述经典疫苗相反,如果疫苗不能诱导特异性针对某种病毒的中和抗体,那么该病毒就很难通过疫苗免疫来预防。以艾滋病为例,尽管美国国立卫生院
(NIH)
每年投入约6亿美元经费用于研发HIV疫苗
[7
]
,目前的HIV候选疫苗依然难以在体内诱导中和抗体。首先,HIV候选疫苗容易诱导机体产生大量“非中和抗体”,这种抗体没有中和活性,因此无法抵御病毒感染细胞。其次,HIV病毒表面的结构蛋白带有大量的糖
(约和蛋白自重相等)
,人体内即使存在中和抗体,也难以通过重重阻隔,无法触碰到病毒。最后,能够产生中和抗体的B细胞往往被自身免疫系统误认为是过敏反应B细胞,从而在早期阶段就被扼杀在摇篮之中
[8
]
。这些技术上的原因往往是病毒本身的性质所决定的。
第二是经济和社会学的原因。
疫苗需要通过临床前试验、I、II、III期临床试验证明安全有效才能上市,因此开发一种疫苗需要耗费大量的财力和人力。尤其是大规模III期临床实验,往往需要上万名受试者,持续3-5年时间,花费大约1.5亿~15亿美元
[9
]
,而且要承受失败的风险。因此,如果公司规模不够大,又没有政府参与和投入,一个制药公司往往难以承担如此昂贵的成本和如此高的风险。即使疫苗通过了III期临床试验得以上市,如果疾病的流行只是区域性的,那么未来该疫苗的市场有可能不足以收回成本。例如,中东冠状病毒
(MERS)
只在阿拉伯半岛和韩国短暂流行
[10
]
,因此,尽管目前MERS的疫苗已经上了I/II期临床试验,且效果可观,但预计完成整个临床试验直至疫苗上市可能还需要十年以上的时间
[11
]
。
针对新型冠状病毒的疫苗,中国疾病预防控制中心主任高福院士在前不久接受采访时说:“大家知道,研发一个疫苗、研究一个疫苗是需要很长很长时间的,但是从我们过去对SARS或者对这一类病毒的认知,我可以拍着胸口讲,这个疫苗肯定会成功的。”
[12
]
美国国立卫生院国家过敏和传染病研究所
(NIAID)
院长Anthony Fauci也向媒体宣布,NIAID将于mRNA疫苗巨头Moderna合作,希望在三个月将新型冠状病毒疫苗推向临床试验。
[13















