正文
Ayres博士出身平凡,父亲是德国移民的普通农民,母亲是记账员。十几岁时,她就开始给杂货店打工,卖冰淇淋。在伯克利大学(Berkeley University)读大学时,她每天花几小时路程去一个实验室全职做研究,毕业时还是拿到了4.0的平均绩点。2009年,她从斯坦福大学博士毕业,导师对她的评价是
“每天花几小时在路上,仍然完成如此大量的研究。她工作相当卖力。”
Ayres博士自己却对于能够在Salk Institute做研究感到非常幸运。这个海边的研究所布满水泥柚木建筑,1960年代,这里是唯一一个实验室之间不设围墙的研究所。正是在这里,她能够和许多神经学和代谢学的专家们自由交流,她自己的研究才会进展得如此顺利。

▲
Salk Institute是美国最著名的生物研究所之一(图片来源:Salk Institute官网)
对科研的全身心付出终于换来回报和认可。2014年,Ayres教授作为15个美国年轻科学家之一,被任命为Searle学者。2015年,她获得五角大楼国防高级研究项目署(DARPA)颁发的年轻学者奖。两个奖项总共带来了80万美元的研究经费,使她能够继续做感兴趣的事业。
对付细菌是一场不会赢的战争
世界范围内,耐药感染的发病率不断上升,每年有高达70万人死于耐药感染。2014年,院内采集的大肠杆菌(一种常见的肠道细菌)样本中,青霉素对60%的样本无效,约25%的样本对其他常用的抗生素中的一种或两种产生耐药。最近,
世界卫生组织首次发布了12种被列为最高优先级的超级细菌名单。
“抗生素耐药不断增强,我们可以用来对付耐药菌的工具差不多用完了,”世卫组织健康体系与研发助理总干事Marie-Paule Kieny博士表示担忧,“抗生素的研发候选物基本枯竭”。
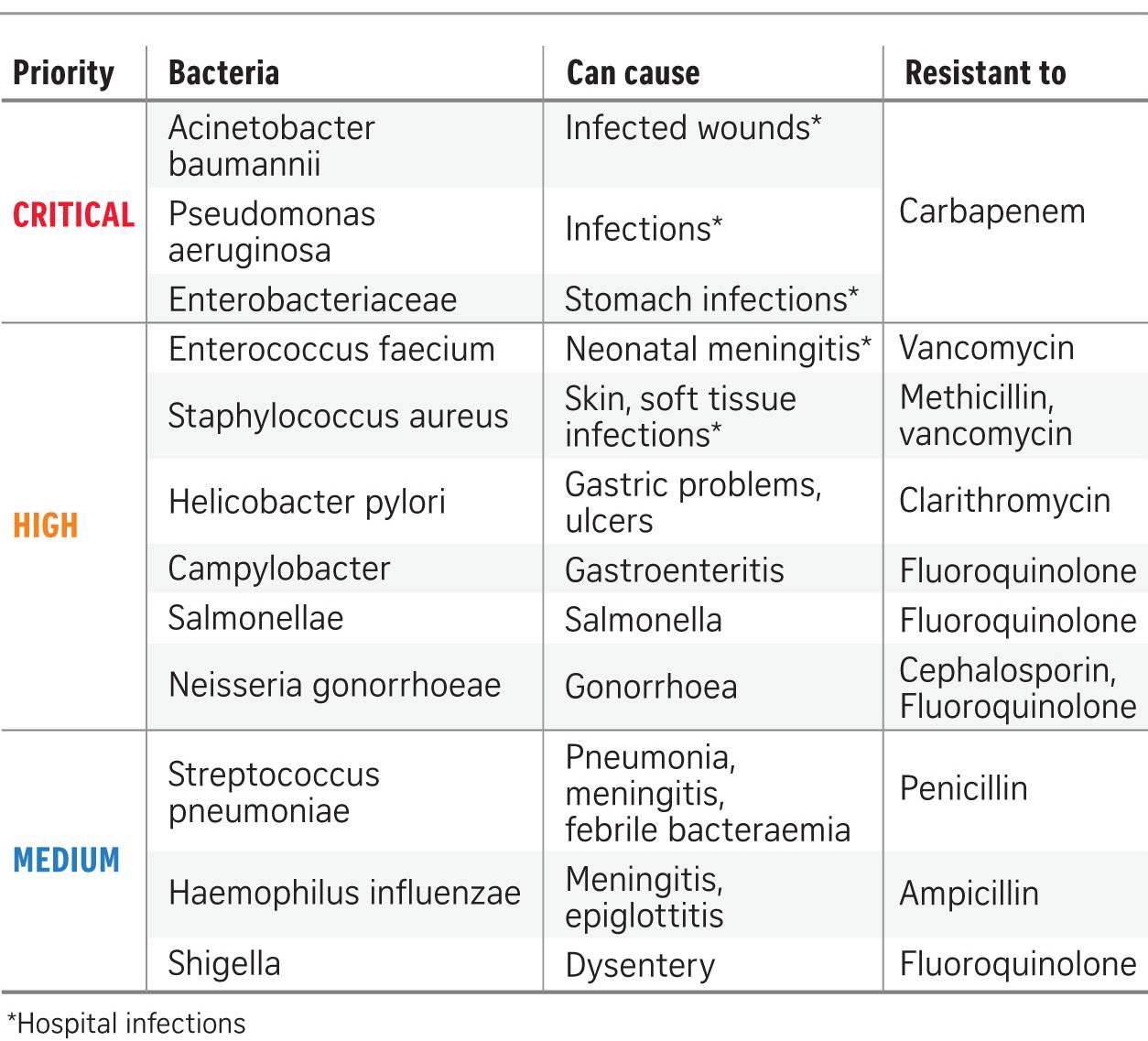
▲
世界卫生组织2017年2月公布的优先病原菌新抗生素研发清单(图片来源:straitstimes)
目前,公共卫生机构的做法是是呼吁新的更有效的抗生素。美国和英国在未来三年将投资数千万美元用于新型抗生素开发。今年4月,美国国会提出了一项法案,其中包括20亿美元的新抗生素研究专项资金。
Ayres博士对这些做法感到叹息。她十分了解细菌,尊重细菌甚至爱上细菌。她知道
它们永远都会赢
。
她认为,社会需要的药物不应该对付细菌,因为
细菌可以进化出逃避最好的抗生素的机制
。相反,我们可以利用细菌甚至病原体,制作靶向感染者的组织和器官的药物,从而挽救生命。这将是一种全新的治疗方法,可以减少对抗生素的依赖,在某些情况下拯救患者,就像她的父亲。
传播这个新的思想并不容易,很多业内科学家对这个新的领域不甚了解。但是
情况正在逐渐转好。
除了细菌感染,
这个新思路对开发其他疾病领域的治疗药物也有帮助
,比如病毒感染,甚至癌症。Schneider教授注意到,有些患者在肿瘤负荷很大的情况下依然生存良好,有些患者却会被很小的肿瘤打垮,帮助患者从放化疗中恢复食欲和力气的药物对提高生存率似乎有效。
业界有一些小型生物技术公司已经在从事这类药物的研发。Ayres博士仍然在自己的实验室里孜孜不倦地进行基础科研,通过一系列研究发现若干新药靶标。她的关注点是微生物组,这是居住在我们体内但却不会导致感染的数万亿细菌的组合。Ayres博士猜测
微生物组可能在“耐受防御系统”中发挥关键作用
。
但是,如果细菌确实有助于增加疾病耐受性,那究竟是什么样的菌株在发挥作用呢?

▲
Ayres教授和她的实验室研究人员(图片来源:Salk Institute官网)
Ayres博士和研究人员正在寻求答案。他们研究
小鼠对肠道感染和沙门氏菌引起的肺炎的反应
。
肠道感染的研究采用的小鼠在遗传特性完全相同,但是由于生长环境不同,所以它们体内具有不同的微生物组。结果发现,尽管所有小鼠感染的病原体数量一样,有一组小鼠没有出现肌肉萎缩,这表明其体内微生物组中的某些物质正在促进疾病耐受性。
研究人员将这些耐受性小鼠的微生物组与普通小鼠进行比较,发现只有
耐受性小鼠携带了特异性的大肠杆菌菌株
,Ayres博士称之为“超级英雄菌”。当他们把“英雄菌株”输给普通小鼠时,竟然也能使这些小鼠避免肌肉萎缩。
通过进一步研究,Ayres博士的研究团队还揭示了
大肠杆菌滋养肌肉的机制
。大肠杆菌可以离开肠道并迁移到脂肪组织,在那里激活免疫系统的炎性体,后者可以刺激炎症反应来对抗微生物感染。
这项研究成果2015年发表在《科学》杂志(相关阅读:Disease tolerance mediated by microbiome E. coli involves inflammasome and IGF-1 signaling. Science.)。
在小鼠实验中获得新发现之后,Ayres博士现在着手研究人体内发挥类似作用的细菌,
希望可以用于肌肉萎缩治疗。
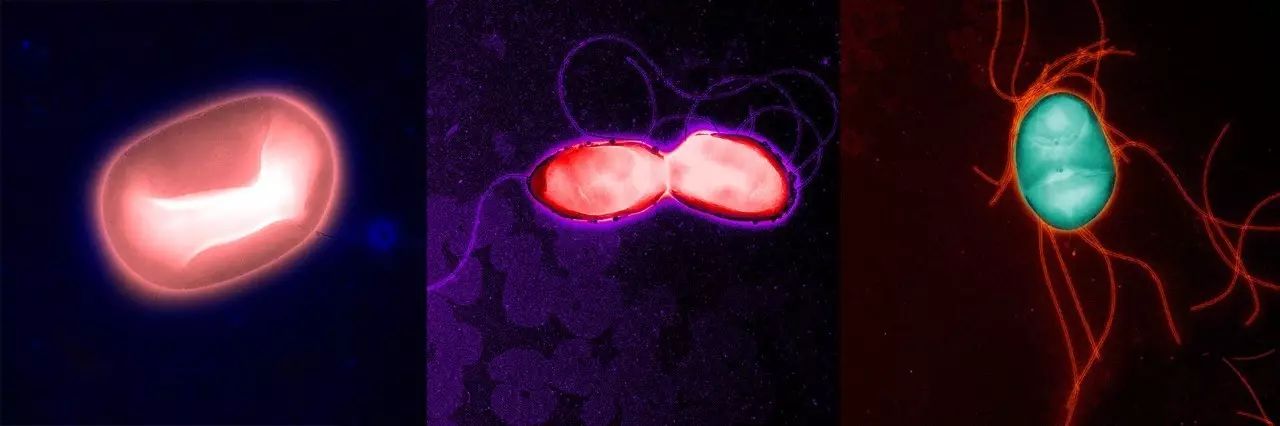
▲
Ayres博士及团队发现一种“超级英雄菌”——大肠杆菌菌株(左),能够阻止感染鼠伤寒沙门氏菌(右)和泰国伯克霍尔德氏菌(中)的小鼠肌肉萎缩。(图片来源:Salk Institute官网)
在另一项研究中
,Ayres博士发现一
种称为SlrP的细菌蛋白可以防止小鼠死于沙门氏菌感染
。研究先通过基因突变获得不含SlrP蛋白的沙门氏菌突变菌株,然后用野生菌株和突变菌株同时去感染小鼠。结果发现,跟感染野生菌株的小鼠相比,感染突变菌株的小鼠吃得更少,体重减轻,死亡更快。
同样, Ayres博士的团队通过进一步研究揭示了野生沙门氏菌中的SlrP蛋白的作用机制,它能够阻断肠道向大脑发送停止进食的信号,使得已经感染沙门氏菌的小鼠能够良好进食 。
研究人员解释说:“
沙门氏菌实际上已经进化出了保持人体健康的方法。
细菌这样做的既得利益是:只要人类继续吃饭和活动,细菌就能继续繁殖并传播给其他宿主。”
这项研究成果2017年发表在《细胞》杂志(相关阅读:Pathogen-Mediated Inhibition of Anorexia Promotes Host Survival and Transmission. Cell.)。
Ayres博士希望这个新发现能够
开发成提高化疗患者食欲的SlrP靶点药物
。
Ayres博士正在努力推动细菌耐受性的基础科学研究,她坚信这会带来新的治疗方法,可以治愈她父亲的细菌感染。














